К ВОПРОСУ О ВЫБОРЕ ДОЗЫ И МЕТОДА ОЦЕНКИ АКТИВНОСТИ НИЗКОМОЛЕКУЛЯРНЫХ ГЕПАРИНОВ ДЛЯ ПРОФИЛАКТИКИ ВЕНОЗНЫХ ТРОМБОЭМБОЛИЧЕСКИХ ОСЛОЖНЕНИЙ В КОМПЛЕКСНОЙ ТЕРАПИИ СИНДРОМА ГИПЕРСТИМУЛЯЦИИ ЯИЧНИКОВ
Зазерская И.Е., Осипова Н.А., Вавилова Т.В., Барабанова Л.В., Конради К.С. Дата публикации на сайте: 2014-11-13 Доступна также в печатной версии журнала Резюме | Полный текст | Скачать в PDF
Резюме:
Синдром гиперстимуляции яичников (СГЯ) – ятрогенное осложнение, проявляющееся в виде гиперергической реакции яичников на применяемые стимуляторы овуляции. В основе клинических проявлений СГЯ лежит резкое повышение сосудистой проницаемости, приводящее к массивному выходу жидкости в межклеточное пространство. Активная экссудация плазмы крови наряду с системной воспалительной реакцией обусловливает в т.ч. развитие гемоконцентрации, повышающей риск тромбозов. В настоящей статье приведены данные современной литературы относительно выбора дозы и длительности применения низкомолекулярных гепаринов для профилактики венозных тромбэмболических осложнений у пациенток с СГЯ.
VENOUS THROMBOEMBOLISM IN RELATION TO OVARIAN HYPERSTIMULATION SYNDROME: AN APPROACH TO DETERMINING THE LOW-MOLECULAR-WEIGHT-HEPARIN DOSES AND ACTIVITY Zazerskaya I.E., Osipova N.A., Vavilova T.V., Barabanova L.V., Konradi K.S.
Almazov Federal Heart, Blood and Endocrinology Centre, Saint-Petersburg
Abstract: ovarian hyperstimulation syndrome (OHSS) is a relatively common complication of ovarian stimulation. The pathophysiology of OHSS is characterised by increased capillary permeability. As a consequence of this, there is a fluid shift into third-space causing hemoconcentration, it may contribute to hypercoagulable state, with increased risk of venous thromboembolism. The article presents modern data on prevention of thromboembolic complication in OHSS patients with special focus on dosage and duration of thromboprophylaxis.
Key words: ovarian hyperstimulation syndrome, thromboprophylaxis, low-molecular-weight-heparin.
Ключевые слова: синдром гиперстимуляции яичников, тромбопрофилактика, низкомолекулярный гепарин.
ФГБУ ФМИЦ им. В.А. Алмазова, Санкт-Петербург
Синдром гиперстимуляции яичников (СГЯ) принято определять как ятрогенное осложнение, проявляющееся в виде гиперергической реакции яичников на применяемые стимуляторы овуляции [3,15]. В основе клинических проявлений СГЯ лежит резкое повышение сосудистой проницаемости, приводящее к массивному выходу жидкости в межклеточное пространство. Активная экссудация плазмы крови обусловливает в т.ч. развитие гемоконцентрации, повышающей риск тромбозов [4,11]. Профилактика венозных тромбоэмболических осложнений (ВТЭО) низкомолекулярными гепаринами (НМГ) является одним из направлений в комплексной терапии СГЯ, однако вопрос о выборе дозы препаратов и длительности их применения остается открытым [9,10,14,25,28]. В настоящей статье приведены данные современной литературы по обсуждаемому вопросу.
Впервые синдром гиперстимуляции яичников был описан в 1943 г., как «syndrome d’hyperluteinisation massive des ovaries», и первый летальный исход от почечной недостаточности (ПН) при СГЯ зафиксирован в 1951 г. [12]. В настоящее время в связи с интенсивным развитием вспомогательных репродуктивных технологий риск развития СГЯ постоянно возрастает.
Частота возникновения СГЯ, по данным различных авторов, очень разнообразна. В более ранних работах синдром средней степени тяжести встречается в 8-23% случаев, а тяжелый – от 0,008 до 10% [26]. По данным Научного центра акушерства, гинекологии и перинатологии РАМН (2005), частота возникновения тяжелой формы синдрома зависит от протокола суперовуляции и колеблется от 9 до 15% [3]. Смертность составляет 1/450000-500000 пациентов [16].
С учетом начала клинических проявлений выделяют раннюю (р-СГЯ) и позднюю (п-СГЯ) формы СГЯ.
Центральным звеном патогенеза как р-СГЯ, так и п-СГЯ является усиление эффектов ряда системных регулирующих биологически активных веществ, избыточно продуцируемых гормонально-зависимыми структурами яичников в случаях повышения чувствительности рецепторного аппарата таких структур
к влиянию фолликулостимулирующего гормона (ФСГ) и/или хорионического гонадотропина (ХГ) [22,29]. При этом для р-СГЯ на фоне быстрого нарастания уровня эстрадиола (Е2) типично увеличение чувствительности яичников одновременно к ФСГ и ХГ. Для п-СГЯ характерно увеличение чувствительности только к ХГ.
Причиной избыточной чувствительности гормонально-зависимых структур яичников к ФСГ и/или к ХГ, вероятно, является увеличение плотности экспрессии или конформационные изменения соответствующих типов рецепторов, усиливающие их воспринимающую и трансмиттерную функции [17,19]. Последствием этого становится гиперергическая реакция яичников на повышение уровня ФСГ и/или ХГ, которая проявляется в виде активной продукции системных регулирующих биологически активных веществ, потенцирующих увеличение проницаемости сосудистого эндотелия в оболочках серозных полостей. К таким биологически активным веществам относят многие интерлейкины (IL-1, -6, -8, -10), ангиотензин-III [13,20], а также сосудисто-эндотелиальный фактор роста (VEGF) [2,22,29]. Перечисленные субстанции способствуют усилению экссудации за счет активации локального образования простагландинов, гистамина, оксида азота и других медиаторов воспаления, непосредственно увеличивающих порозность эндотелия сосудов [5]. В связи с их повышенной проницаемостью происходит массивный выход плазмы во внесосудистое пространство, что приводит к гиповолемии и гемоконцентрации, большим потерям белка, формированию полисерозитов, нарушению почечной перфузии, нарушению функции печени, развитию респираторного дистресс-синдрома взрослых, венозным тромбоэмболическим осложнениям (ВТЭО).
Развитию ВТЭО при СГЯ способствуют высокая концентрация половых стероидных гормонов и повреждение эндотелия сосудистой стенки [30]. Точная частота тромбоэмболий не известна. По данным литературы, данное осложнение возникает примерно у 10% пациенток с тяжелой формой СГЯ. В структуре тромбозов при синдроме преобладают венозные (75%). Наиболее часто диагностируют тромбозы глубоких вен, яремной, подключичной и нижней полой вен. Частота артериальных тромбозов составляет около 25%. Могут поражаться церебральные, позвоночные, подключичные артерии, нижняя сонная артерия, бедренные и брыжеечные артерии, аорта [3,17,31,32].
Согласно федеральным клиническим рекомендациям антитромботическая терапия показана при появлении лабораторных признаков гиперкоагуляции, а именно – при повышении концентрации D-димера в плазме крови, которое обычно сочетается с повышением уровня фибриногена. Длительность терапии НМГ определяется нормализацией уровня D-димера и при беременности может превышать 30 дней [9]. У пациенток с СГЯ риск развития тромбоза в первом триместре увеличивается в 100 раз по сравнению с женщинами, у которых беременность наступила в естественном цикле [25]. В связи с этим при СГЯ средней и тяжелей степени тромбопрофилактику целесообразно продолжать до конца первого триместра, если беременность наступила, или до разрешения симптомов гиперстимуляции яичников, если беременность не наступила [14]. Решение о продолжении терапии антикоагулянтами во втором и третьем триместрах, а также в послеродовом периоде принимают на основании оценки индивидуальных факторов риска (см. табл. 1).
Таблица 1. Оценка риска венозных тромбоэмболических осложнений (ВТЭО) во время беременности, RCOG, 2009 [24].
1. Единственный предшествующий эпизод ВТЭО+тромбофилия или наследственный характер ВТЭО, не связанный с приемом эстрогенов
2. Предшествующие или текущие ВТЭО (>1) | Высокий риск ВТЭО | Требуется профилактика
НМГ в течение всей беременности
Применение компрессионного трикотажа | 1. Единственный предшествующий эпизод ВТО без семейной истории или тромбофилии
2. Тромбофилии без тромбозов
3. Наличие сопутствующей соматической патологии
4. Хирургические операции во время беременности | Средний риск ВТЭО | Рекомендуется профилактика
НМГ на усмотрение врача, исходя из клинической ситуации
Применение эластического трикотажа | 1. Возраст >35лет
2. Избыточная масса тела (ИМТ >30)
3. Паритет >3
4. Варикозная болезнь вен нижних конечностей
5. Курение
6. Длительная иммобилизация
7. Преэклампсия
8. Многоплодная беременность или ЭКО)
9. Дегидратация
10. Синдром гиперстимуляции яичников | Если три и более фактора или два фактора+клиническая ситуация, то средний риск ВТЭО
Если менее трех факторов – низкий риск | | Если менее трех факторов – низкий риск ВТЭО | НМГ не требуются
Применение компрессионного трикотажа
Мобилизация и предупреждение дегидратации |
Примечание. НМГ – низкомолекулярный гепарин; ИМТ – индекс массы тела.
При этом нет указаний на необходимость проводить какие-либо гемостазиологические тесты ни перед началом терапии, ни для оценки ее эффективности [14,24].
Нет единого мнения и относительно дозы НМГ. Согласно федеральным клиническим рекомендациям профилактика тромбоэмболических осложнений проводится лечебной дозой НМГ. Эффективную и обладающую достаточным профилем безопасности лечебную дозу НМГ целесообразно подбирать индивидуально, в зависимости от массы тела пациентки и уровня ингибиторной активности плазмы к фактору Ха (анти-Ха-активность) плазмы крови, определенного через 3 ч после инъекции препарата и соответствующего времени максимальной активности НМГ [9]. Действительно, для оценки эффективности и безопасности лечебных доз антикоагулянтов должны использоваться специальные тесты (нефракционированный гепарин – АЧТВ, низкомолекулярный – анти-Xа активность) [1,8], однако в литературе нет указаний на необходимость определения анти-Xа активности при использовании профилактических и максимальных профилактических доз НМГ [8,14,28]. Максимальные профилактические дозы, обеспечивающие анти-Xa-активность в крови от 0,1 до 0,3 ЕД/мл, для далтепарина составляют 5000 МЕ подкожно 2 раза в сут., для эноксапарина – подкожно 40 мг 2 раза в сут., для надропарина – 0,3 мл 2 раза в сут. [1].
Гепарин является катализатором связывания антитромбином нескольких ферментов, участвующих в процессах свертывания крови. Соединяясь с молекулой антитромбина, молекула гепарина вызывает изменения последней, в результате чего как минимум в 1000 раз увеличивается способность активного центра антитромбина взаимодействовать с рядом активированных факторов свертывания крови. Образуя комплекс с антитромбином, эти ферменты перестают участвовать в процессе коагуляции, что, в конечном итоге, приводит к уменьшению числа молекул тромбина. Нефракционированный гепарин (НФГ) – гетерогенная смесь полисахаридов со средней молекулярной массой 15 000 дальтон. В отличие от НФГ низкомолекулярный гепарин (НМГ) имеет короткие полисахаридные цепи (менее 18 моносахаридов), что значительно увеличивает биодоступность препарата при подкожном введении и обеспечивает более медленный клиренс, который осуществляется преимущественно почками. Кроме этого, НМГ по сравнению с НФГ теряет часть антитромбиновой активности, взамен приобретая способность селективно подавлять фактор Ха, благодаря чему риск геморрагических осложнений значительно снижается (см. рис. 1).
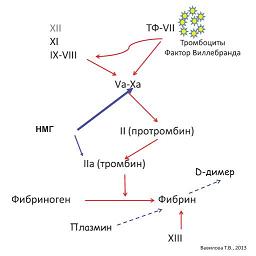 | Рисунок 1: Коагуляционный гемостаз.
Синими стрелками показана точка приложения действия НМГ: снижение антитромбиновой активности (IIa) и способность селективно подавлять фактор Ха. |
Повышение безопасности и эффективности НМГ связано с уменьшением их молекулярной массы и обеспечением однородности полисахаридных цепей. Работы в этом направлении привели к созданию второй генерации НМГ, представителем которой является бемипарин. Бемипарин натрий (бемипарин) представляет собой НМГ, получаемый путем щелочной деполимеризации (р-элиминация) НФГ, экстрагируемого из слизистой оболочки кишечника свиней. Бемипарин обладает самой низкой среди НМГ средней молекулярной массой 3600 Да и однородностью молекулярных цепей, 85% которых весят менее 6000 Да. В Российской Федерации бемипарин (коммерческое название Цибор®) зарегистрирован для использования в целях профилактики ВТЭО и предупреждения свертывания крови в системах экстракорпорального кровообращения [6] при проведении гемодиализа, хотя есть данные об эффективном и безопасном применении этого препарата в акушерской практике. Так, в проспективное исследование, проведенное K.W. Sharif, S. Ghunaim [27], были включены 273 женщины младше 40 лет, перенесшие ранее неудачные имплантации. Пациенткам с тромбофилией выполнялась тромбопрофилактика бемипарином в дозе 3500 МЕ/сут. В итоге уровень удачных повторных имплантаций в этой группе составил 55%, что позволило предположить положительную роль терапии бемипарином. В исследовании, проведенном И.В. Лыдиной, применение бемипарина натрия привело не только к эффективному снижению тромбогенного потенциала у пациенток в цикле ЭКО, но и значительному (в 6,4 раза) увеличению числа случаев наступления беременности [7].
Таким образом, развитие СГЯ сопряжено со стократным увеличением риска венозных тромбоэмболических осложнений в первом триместре беременности. Пациентки с СГЯ средней и тяжелой степени должны получать профилактику ВТЭО низкомолекулярными гепаринами. Для профилактики могут использоваться профилактическая, максимальная профилактическая или лечебная доза. Тромбопрофилактику целесообразно продолжать до конца первого триместра, если беременность наступила, или до разрешения симптомов гиперстимуляции яичников, если беременность не наступила. Решение о продолжении терапии антикоагулянтами во втором и третьем триместрах, а также в послеродовом периоде принимают на основании оценки индивидуальных факторов риска. При использовании профилактических и максимальных профилактических доз какие-либо гемостазиологические тесты ни перед началом терапии, ни для оценки ее эффективности не проводятся, введение терапевтических доз возможно под контролем анти Ха-активности сыворотки крови.
Литература:
1. Берковский А.Л., Сергеева Е.В., Суворова А.В., Козлова А.А. Методы определения активности гепарина. Методическое руководство. М. 2011; 54 с.
2. Комиссарова Ю.В. Оптимизация программы экстракорпорального оплодотворения и переноса эмбрионов с учетом ангиогенных факторов: автореф. дис. ... канд. мед. наук. М. 2010; 33 с.
3. Корнеева И.Е. Синдро гиперстимуляции яичников. В кн.: Бесплодный брак. Под ред. В.И. Кулакова. М. 2006; 449-496.
4. Корнеева И.Е., Иванова А.В., Баркалина Н.В. Синдром гиперстимуляции яичников: профилактика, диагностика, лечение (обзор литературы). Проблемы репродукции. 2004; 10 (1): 43-50.
5. Кулаков В.И., Калинина Е.А., Корнеева И.Е. и др. Лечение синдрома гиперстимуляции яичников. В кн.: Лечение женского и мужского бесплодия. Вспомогательные репродуктивные технологии. Под ред. В.И. Кулакова, Б.В. Леонова, Л.Н. Кузьмичева. М. 2005; 447-74.
6. Кудыкин М.Н. Цибор® – новый низкомолекулярный гепарин. Хирургия. 2012; 1: 22-25.
7. Лыдина И.В. Опыт использования бемипарина натрия для повышения результативности экстракорпорального оплодотворения. Тромбоз, гемостаз и реология. 2012; 4 (52): 41-44.
8. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. Флебология. 2010; 4 (2): 6-27.
9. Федеральные клинические рекомендации. Диагностика и лечение синдрома гиперстимуляции яичников. М. 2013; 27 с.
10. Bates S.M., Greer I.A., Pabinger I. et al. American College of Chest Physicians. Venous thromboembolism, thrombophilia, antithrombotic therapy, and pregnancy: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest. 2008; 133 (6): 844–86.
11. Binder H., Dittrich R., Einhaus F. et al. Update on ovarian hyperstimulation syndrome: part 2 – clinical signs and treatment. Int J Fertil Womens Med. 2007; 52 (2-3): 69-81.
12. Budev M., Arroliga A., Falcone T. Ovarian hyperstimulation syndrome. Crit. Care. Med. 2005; 33: 301-306.
13. Chen C.D., Chen H.F., Lu H.F. et al. Value of serum and follicular fluid cytokine profile in the prediction of moderate to severe ovarian hyperstimulation syndrome. Hum. Reprod. 2000; 15 (5): 1037-42.
14. Chin-Der Chen, Shee-Uan Chen, Yu-Shih Yang Prevention and management of ovatian hyperstimulation syndrome. Best Practice and Research Clinical Obstetrics and Gynaecology. 2012; 26: 812-27.
15. Delvigne A., Rozenberg S. Review of clinical course and treatment of ovarian hyperstimulation syndrome (OHSS). Hum. Reprod. Update. 2003; 9 (1): 77-96.
16. Delvigne A., Rozenberg S. Epidemiology and prevention of ovarian hyperstimulation syndrome (OHSS). A review. Hum. Reprod. 2002; 8: 559-77.
17. Delvigne A., Kostyla K., De Leener A. et al. Metabolic characteristics of women who developed ovarian hyperstimulation syndrome. Hum. Reprod. 2002;17 (8): 1994-96.
18. Delvigne A., Rozenberg S. Review of clinical course and treatment of ovarian hyperstimulation syndrome (OHSS). Hum. Reprod. 2003; 9: 77-96.
19. Garcia-Velasco J., Pellicer A. New concepts in the understanding of the ovarian hyperstimulation syndrome. Curr. Opin. Obstet. Gynecol. 2003; 15: 251-56.
20. Garcia-Velasco J.A., Ariel J.A. Chemokines in human reproduction: immune system interactions. Immunol. Clin. N. Am. 2002; 13: 127-44.
21. Kerkela E., Skottman H., Friden B. et al. Exclusion of coding-region mutations in luteinizing hormone and follicle-stimulating hormone receptor genes as the cause of ovarian hyperstimulation syndrome. Fertil. Steril. 2007; 87 (3): 603-6.
22. Manau D., Fabregues F., Penarrabia J. Vascular endothelial growth factor levels in serum and plasma from patients undergoing controlled ovarian hyperstimulation for IVF. Hum. Reprod. 2007; 22: (3): 669-75.
23. Rizk B. Symposium: Update on prediction and management of OHSS. Genetics of ovarian hyperstimulation. Reprod. Bio.Med. Online. 2009; 19 (1): 14-27.
24. Royal College of Obstetricians and Gynaecologists. Reducing the risk of thrombosis and embolism during pregnancy and the puerperium Green-top. Guideline. 2009; 37a.
25. Rova K., Passmark H., Lindqvist P.G Venous thromboembolism in relation to in vitro fertilization: an approach to determinihg the incidence and increase in risk in succrssful cycles. Fertil. Steril. 2012; 97 (1): 95-100.
26. Schenker J., Weinstein D. Ovarian hyperstimulation syndrome: A current survey. Fertil. Steril. 1978; 30: 255-68.
27. Sharif K.W., Ghunaim S. Management of 273 cases of recurrent implantation failure: results of a combined evidence-based protocol. Reprod Biomed Online. 2010 Sep; 21 (3): 373-80.
28. Shmorgun D., Claman P. The diagnosis and management of ovarian hyperstimulation syndrome. J Obstet. Gynaecol. 2011; 11: 1156-1162.
29. Soares S.R., Gomez R., Simon С. et al. Targeting the vascular endothelial growth factor system to prevent ovarian hyperstimulation syndrome. Hum. Reprod. Update. 2008; 14 (4): 321-33.
30. Stewart J., Hamilton P., Murdoch A. Thromboembolic disease associated with ovarian hyperstimulation and assisted conception techniques. Hum. Reprod. 1997; 12: 2167-73.
31. The management of ovarian hyperstimulation syndrome. Setting standards to improve womens health. Royal College of Obstetricians and Gynaecologists. Green-top Guideline; 2006. 11 p.
32. The Practice Committee of the American Society for Reproductive Medicine. Ovarian hyperstimulation syndrome. Fertil. Steril. 2004; 82: 81-86.
References:
1. Berkovskii A.L., Sergeeva E.V., Suvorova A.V., Kozlova A.A. Methods for determining the activity of heparin. Methodological guidance [Metody opredeleniya aktivnosti geparina. Metodicheskoe rukovodstvo]. Moscow. 2011; 54 s.
2. Komissarova Yu.V. Optimizatsiya programmy ekstrakorporal’nogo oplodotvoreniya i perenosa embrionov s uchetom angiogennykh faktorov: avtoref. dis. ... kand. med. nauk (Optimization program of in vitro fertilization and embryo transfer with the angiogenic factors) Phd. diss. Moscow. 2010; 33 s.
3. Korneeva I.E. Ovarian hyperstimulation syndrome. In .: sterile marriage. Ed. VI Kulakov [Sindrom giperstimulyatsii yaichnikov. V kn.: Besplodnyi brak. Pod red. V.I. Kulakova]. Moscow. 2006; 449-496.
4. Korneeva I.E., Ivanova A.V., Barkalina N.V. Problemy reproduktsii. 2004; 10 (1): 43-50.
5. Kulakov V.I., Kalinina E.A., Korneeva I.E. i dr. Treatment of ovarian hyperstimulation syndrome. In .: Treatment of female and male infertility. Assisted reproductive technology. Ed. VI Kulakov, BV Leonova, LN Kuz’micheva [Lechenie sindroma giperstimulyatsii yaichnikov. V kn.: Lechenie zhenskogo i muzhskogo besplodiya. Vspomogatel’nye reproduktivnye tekhnologii. Pod red. V.I. Kulakova, B.V. Leonova, L.N. Kuz’micheva]. Moscow. 2005; 447-74.
6. Kudykin M.N. Khirurgiya. 2012; 1: 22-25.
7. Lydina I.V. Tromboz, gemostaz i reologiya. 2012; 4 (52): 41-44.
8. Russian clinical recommendations for diagnosis, treatment and prevention of venous thromboembolic events. Flebologiya. 2010; 4 (2): 6-27.
9. Federal clinical guidelines. Diagnosis and treatment of ovarian hyperstimulation syndrome [Federal’nye klinicheskie rekomendatsii. Diagnostika i lechenie sindroma giperstimulyatsii yaichnikov]. Moscow. 2013; 27 s.
10. Bates S.M., Greer I.A., Pabinger I. et al. American College of Chest Physicians. Venous thromboembolism, thrombophilia, antithrombotic therapy, and pregnancy: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest. 2008; 133 (6): 844–86.
11. Binder H., Dittrich R., Einhaus F. et al. Update on ovarian hyperstimulation syndrome: part 2 – clinical signs and treatment. Int J Fertil Womens Med. 2007; 52 (2-3): 69-81.
12. Budev M., Arroliga A., Falcone T. Ovarian hyperstimulation syndrome. Crit. Care. Med. 2005; 33: 301-306.
3. Chen C.D., Chen H.F., Lu H.F. et al. Value of serum and follicular fluid cytokine profile in the prediction of moderate to severe ovarian hyperstimulation syndrome. Hum. Reprod. 2000; 15 (5): 1037-42.
14. Chin-Der Chen, Shee-Uan Chen, Yu-Shih Yang Prevention and management of ovatian hyperstimulation syndrome. Best Practice and Research Clinical Obstetrics and Gynaecology. 2012; 26: 812-27.
15. Delvigne A., Rozenberg S. Review of clinical course and treatment of ovarian hyperstimulation syndrome (OHSS). Hum. Reprod. Update. 2003; 9 (1): 77-96.
16. Delvigne A., Rozenberg S. Epidemiology and prevention of ovarian hyperstimulation syndrome (OHSS). A review. Hum. Reprod. 2002; 8: 559-77.
17. Delvigne A., Kostyla K., De Leener A. et al. Metabolic characteristics of women who developed ovarian hyperstimulation syndrome. Hum. Reprod. 2002;17 (8): 1994-96.
18. Delvigne A., Rozenberg S. Review of clinical course and treatment of ovarian hyperstimulation syndrome (OHSS). Hum. Reprod. 2003; 9: 77-96.
19. Garcia-Velasco J., Pellicer A. New concepts in the understanding of the ovarian hyperstimulation syndrome. Curr. Opin. Obstet. Gynecol. 2003; 15: 251-56.
20. Garcia-Velasco J.A., Ariel J.A. Chemokines in human reproduction: immune system interactions. Immunol. Clin. N. Am. 2002; 13: 127-44.
21. Kerkela E., Skottman H., Friden B. et al. Exclusion of coding-region mutations in luteinizing hormone and follicle-stimulating hormone receptor genes as the cause of ovarian hyperstimulation syndrome. Fertil. Steril. 2007; 87 (3): 603-6.
22. Manau D., Fabregues F., Penarrabia J. Vascuar endothelial growth factor levels in serum and plasma from patients undergoing controlled ovarian hyperstimulation for IVF. Hum. Reprod. 2007; 22: (3): 669-75.
23. Rizk B. Symposium: Update on prediction and management of OHSS. Genetics of ovarian hyperstimulation. Reprod. Bio.Med. Online. 2009; 19 (1): 14-27.
24. Royal College of Obstetricians and Gynaecologists. Reducing the risk of thrombosis and embolism during pregnancy and the puerperium Green-top. Guideline. 2009; 37a.
25. Rova K., Passmark H., Lindqvist P.G Venous thromboembolism in relation to in vitro fertilization: an approach to determinihg the incidence and increase in risk in succrssful cycles. Fertil. Steril. 2012; 97 (1): 95-100.
26. Schenker J., Weinstein D. Ovarian hyperstimulation syndrome: A current survey. Fertil. Steril. 1978; 30: 255-68.
27. Sharif K.W., Ghunaim S. Management of 273 cases of recurrent implantation failure: results of a combined evidence-based protocol. Reprod Biomed Online. 2010 Sep; 21 (3): 373-80.
28. Shmorgun D., Claman P. The diagnosis and management of ovarian hyperstimulation
syndrome. J Obstet. Gynaecol. 2011; 11: 1156-1162.
29. Soares S.R., Gomez R., Simon S. et al. Targeting the vascular endothelial growth factor system to prevent ovarian hyperstimulation syndrome. Hum. Reprod.Update. 2008; 14 (4): 321-33.
30. Stewart J., Hamilton P., Murdoch A. Thromboembolic disease associated with ovarian hyperstimulation and assisted conception techniques. Hum. Reprod. 1997; 12: 2167-73.
31. The management of ovarian hyperstimulation syndrome. Setting standards to improve women’s health. Royal College of Obstetricians and Gynaecologists. Green-top Guideline; 2006. 11 p.
32. The Practice Committee of the American Society for Reproductive Medicine. Ovarian hyperstimulation syndrome. Fertil. Steril. 2004; 82: 81-86.
Venous thromboembolism in relation to ovarian hyperstimulation syndrome: an approach to determining the low-molecular-weight-heparin doses and activity
Zazerskaya I.E., Osipova N.A., Vavilova T.V., Barabanova L.V., Konradi K.S.
Almazov Federal Heart, Blood and Endocrinology Centre, Saint-Petersburg
Abstract: ovarian hyperstimulation syndrome (OHSS) is a relatively common complication of ovarian stimulation. The pathophysiology of OHSS is characterised by increased capillary permeability. As a consequence of this, there is a fluid shift into third-space causing hemoconcentration, it may contribute to hypercoagulable state, with increased risk of venous thromboembolism. The article presents modern data on prevention of thromboembolic complication in OHSS patients with special focus on dosage and duration of thromboprophylaxis.
Key words: ovarian hyperstimulation syndrome, thromboprophylaxis, low-molecular-weight-heparin. |
|