МНОГОПЛОДИЕ. СОВРЕМЕННЫЕ ПОДХОДЫ К ТАКТИКЕ ВЕДЕНИЯ БЕРЕМЕННОСТИ
Сичинава Л.Г. Дата публикации на сайте: 2014-08-14 Доступна также в печатной версии журнала Резюме | Полный текст | Скачать в PDF
Резюме:
В клинической лекции, посвященной принципам ведения беременных с многоплодием, представлены современным методы диагностики, профилактики и лечения осложнений, присущих этой группе пациенток высокого риска. Показана необходимость дифференцированного подхода к ведению многоплодной беременности в зависимости от хориальности, которая определяет перинатальные исходы.
CURRENT APPROACHES TO MANAGEMENT OF MULTIPLE PREGNANCIES
Sichinava L.G.
The Russian National Research Medical University named after N.I. Pirogov of the Ministry of Health of the Russian Federation, Moscow
Abstract: a clinical lecture presents the current management of multiple pregnancies, modern diagnostics and treatment of complications in this high risk group of patients. A different approaches to management of multiple pregnancies according to chorionicity, early diagnosis of specific complications is necessary for improving neonatal outcomes.
Key words: multiple pregnancy, twins, preterm birth, management of twin pregnancy.
Ключевые слова: многоплодная беременность, двойня, преждевременные роды, тактика ведения.
ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава РФ, Москва
Повышенный интерес к многоплодной беременности, как в некотором роде таинству природы, известный еще с древних времен, не ослабевает и в настоящее время. В последние десятилетия проблема многоплодия приобрела особую актуальность. В первую очередь это связано со значительным ростом частоты многоплодной беременности, которая приобрела в мире масштабы «эпидемии». Так, с 1980 по 2009 г. число многоплодных родов в США практически удвоилось (с 18,9 до 33,2 на 1000 родов). Частота многоплодной беременности в большинстве европейских стран колеблется от 0,7 до 1,5%. Возросла она и в России – с 2000 по 2012 г. на 48,6% – с 0,7 до 1,1% (см. рис. 1). Это хорошо видно и на примере мегаполисов – Москвы и Санкт--Петербурга, где частота многоплодных родов составляет 1,4-2,4%. Основными причинами увеличения частоты многоплодной беременности является широкое внедрение в практику вспомогательных репродуктивных технологий (ВРТ), а также т.н. «отложенное» деторождение. Рост частоты многоплодной беременности происходит в основном за счет роста числа двоен; частота троен не увеличивается, а даже снижается в последние годы и, конечно же, это положительный результат административных ограничений по количеству переносимых эмбрионов при проведении ЭКО. Заслуживает внимания тот факт, что неуклонно, как и во всем мире, растет доля индуцированного, т.н. ятрогенного многоплодия, что привело к изменению соотношения спонтанной и индуцированной многоплодной беременности: 70 и 30% в 80-е гг. против 45 и 55% к 2000 г.
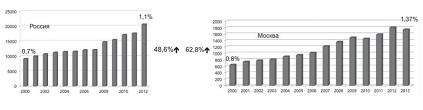 | Рисунок 1: Частота многоплодных родов. |
Многочисленные исследования, посвященные проблеме многоплодной беременности, позволяют расценивать ее как фактор высокого риска неблагоприятных исходов для матери и плода – от 2- до 10-кратного увеличения частоты преждевременных родов, гестоза, преждевременной отслойки плаценты, анемии, задержки роста плода/плодов, внутриутробной гибели плода/плодов и, как результат этого, – более высокие показатели ПС по сравнению с одноплодной беременностью. При этом перинатальные потери при многоплодной беременности возрастают с увеличением числа вынашиваемых плодов. В связи с вышесказанным «эпидемия» МБ ставит перед акушерами и перинатологами важные вопросы, относящиеся к анте- и интранатальному ведению этой группы пациенток высокого риска.
Исходы беременности, даже при многоплодии одного и того же порядка, далеко неодинаковы, и на сегодняшний день неоспоримым является тот факт, что именно хориальность, а не зиготность определяет перинатальные исходы при многоплодии. Наиболее неблагоприятной в плане перинатальных осложнений является монохориальная многоплодная беременность, которая наблюдается в 65% однояйцевой двойни. Сами по себе монохориальные двойни составляют примерно 0,7% от всех беременностей. Перинатальная смертность при монохориальной двойне в 3-4 раза превышает таковую при дихориальной, частота преждевременных родов до 32 нед. почти в 2 раза выше при монохориальном типе плацентации – 9,2 против 5,5%.
Диагноз монохориальности требует подтверждения единой плаценты, тонкой межплодовой перегородки, и отсутствия специфического ультразвукового критерия дихориального типа плацентации – λ--признака (см. рис. 2). Диагноз монохориальности необходимо ставить с осторожностью или вообще не ставить, если невозможно точно установить наличие или отсутствие λ--признака. Оптимальным сроком для определения хориальности (типа плацентации) является 11-14 нед. беременности, когда при выявлении единой «плацентарной массы» нужно дифференцировать единственную плаценту (монохориальная двойня) от двух слившихся (дихориальная двойня). Следует учитывать, что после 15-16 нед. беременности диагностическая значимость λ--признака снижается. Выявление λ--признака на любом сроке при ультразвуковом исследовании указывает на дихориальный тип плацентации.
 | Рисунок 2: Определение хориальности: а) λ-признак – ДХ; б) Т-признак – МХ. |
При многоплодии к организму женщины предъявляются повышенные требования: сердечно-сосудистая система, легкие, печень, почки и другие органы и системы функционируют с большим напряжением. Материнская заболеваемость и смертность при многоплодной беременности в 3-7 раз выше по сравнению с одноплодной; чем выше порядок многоплодия, тем выше риск материнских осложнений. Так, риск развития гестоза у пациенток при многоплодии достигает 45%. При этом гестоз, как правило, возникает в более ранние сроки гестации и протекает тяжелее, чем при одноплодной беременности, что частично объясняется увеличенным объемом плацентарной массы – теория гиперплацентоза (впервые понятие «гиперплацентоз» было введено в клиническую практику в 1959 г. T.N. Jeff-coate и J.S. Scott). Нередко у беременных с многоплодием гипертензия и отеки развиваются вследствие избыточного увеличения внутрисосудистого объема, что ошибочно расценивается как гестоз. В таких случаях скорость клубочковой фильтрации повышена, протеинурия незначительная или отсутствует, а снижение величины гематокрита в динамике указывает на увеличенный объем плазмы.
Немалый вклад в неблагоприятные перинатальные исходы при многоплодии вносит анемия, частота которой у беременных с двойней достигает 50-100%. Анемию часто считают обычным осложнением, связанным с увеличением внутрисосудистого объема. Повышение объема плазмы (в большей степени, чем при одноплодной беременности) приводит к снижению величины гематокрита и уровня гемоглобина, особенно во 2-м триместре беременности. Значительное увеличение эритропоэза во время беременности двойней может привести к истощению ограниченных запасов железа и сыграть роль пускового механизма в развитии железодефицитной анемии, важное место в развитии анемии занимает белковая недостаточность, которая выявляется у 36,2% беременных с многоплодием. Выраженная анемия (Hb менее 80-90 г/л) повышает риск задержки роста плода в 2 раза, преждевременных родов – до 60%, внутриутробной гибели плода – в 3 раза, а также гестоза, железодефицитной анемии у новорожденных. Учитывая, что риск вышеуказанных осложнений изначально высокий у беременных с многоплодием, профилактике анемии у этой группы пациенток придается особое значение. Назначение противоанемической терапии (прием железосодержащих препаратов и фолиевой кислоты) рекомендуется с 16-20 нед. беременности.
Особое значение при многоплодной беременности, независимо от хориальности, приобрела проблема тромбофилии. Даже физиологически протекающая дихориальная двойня сопровождается более выраженной и более ранней (15-18 нед.) гиперкоагуляцией и снижением активности естественных антикоагулянтов по сравнению с одноплодной беременностью, что является фактором повышенного риска тромбогеморрагических осложнений в родах и пуэрперии. Гормональная нагрузка при ЭКО у беременных с ятрогенным многоплодием, частота которого неуклонно возрастает, является дополнительным фактором риска осложненного течения многоплодной беременности при генетической и/или приобретенной тромбофилии. В связи с вышесказанным оправданными являются рекомендации наших отечественных ученых о необходимости скрининга на наличие генетической тромбофилии, антифосфолипидных антител, гипергомоцистеинемии у беременных двойней после ЭКО и при выявлении таковых применение низкомолекулярных гепаринов, как можно с более ранних сроков беременности, с целью улучшения процессов имплантации, инвазии трофобласта и плацентации, а также для профилактики венозного тромбоэмболизма [3].
Течение многоплодной беременности нередко осложняется задержкой роста одного или обоих плодов, частота которой в 10 раз выше таковой при одноплодной беременности и составляет 34 и 23% соответственно при моно- и дихориальной двойне. При монохориальном типе плацентации чаще отмечается задержка роста одного из плодов, в то время как при дихориальном – обоих плодов. По мере прогрессирования многоплодной беременности увеличивается как частота задержки плода/плодов, так и степень выраженности этого осложнения, что в немалой степени объясняется конкурентным сосуществованием плодов.
Одним из факторов, наиболее тесно коррелирующих с массой детей при рождении и, что немаловажно, с продолжительностью беременности является общая прибавка массы тела пациентки. Так, при прибавке до 10 кг задержка роста плода/плодов (ЗРП) была отмечена нами в 100% наблюдений [5]. Это согласуется с данными мировой литературы, по которым оптимальной при двойне, в отличие от одноплодной беременности, является общая прибавка за беременность 20-22 кг, при которой частота ЗРП является наименьшей и составляет 24-28% [9]. При этом акцент надо делать на прибавку массы тела в первую половину беременности – не менее 11-12 кг. Конечно, при этом необходимо учитывать исходный индекс массы тела беременной.
Следует отметить, что оценка физического развития детей при многоплодии до настоящего времени часто проводится на основании нормативов, разработанных для новорожденных от одноплодной беременности, что затрудняет верификацию диагноза гипотрофии, приводя как к завышению, так и к занижению ее частоты, и, таким образом, к нерациональной тактике ведения детей из двойни в неонатальном периоде. Учитывая все вышесказанное, нами были разработаны нормативные параметры физического развития новорожденных из дихориальной двойни на основании комплексного обследования 796 детей, родившихся у 398 пациенток в сроки от 32 до 40 нед. гестации. Результаты нашего исследования показали, что величина массоростового показателя для детей из двойни, независимо от гестационного возраста, ниже такового у новорожденных от одноплодной беременности. Для новорожденных из двойни, родившихся в 37 и более нед. гестации, величина массоростового индекса колеблется от 55 до 60, в то время как для доношенных детей от одноплодной беременности он находится в пределах от 59 до 68, что необходимо учитывать при оценке параметров физического развития двоен и, в особенности, для обоснованной диагностики гипотрофии [2].
Прогностически наиболее неблагоприятной является т.н. селективная задержка роста одного из плодов при монохориальной двойне, когда различие в предполагаемой массе достигает 25% и более, частота этого осложнения составляет около 7%. Пациентки с монохориальной двойней и селективной задержкой роста плода требуют особо тщательного ультразвукового динамического контроля за состоянием обоих плодов. На основании допплерометрии кровотока в артерии пуповины у плодов с селективной задержкой роста выделяют три типа задержки; при 2-м и 3-м типах, которые характеризуются отсутствием диастолического компонента (постоянным или преходящим) резко возрастает риск внезапной внутриутробной гибели и/или неврологических осложнений у детей.
Наряду с монохориальным типом плацентации основная причина неблагоприятных перинатальных исходов при многоплодии – это недоношенность. Одним из наиболее частых осложнений многоплодной беременности являются преждевременные роды. Обсуждая проблему преждевременных родов, нельзя не отметить, что одной из основных причин увеличения частоты преждевременных родов в развитых странах является широкое внедрение вспомогательных репродуктивных технологий и, таким образом, опосредованно – рост ятрогенного многоплодия. При этом следует отметить, что частота преждевременных родов на 23% выше при беременности, наступившей в результате ЭКО по сравнению с таковой при спонтанной двойне. Около половины беременностей двойней и до 80% тройней прерываются до 36 недель. При этом, чем больше число вынашиваемых плодов, тем выше риск преждевременного прерывания беременности. Так, при двойне роды, как правило, наступают в 36-37 нед., при тройне – в 33-34 нед., при четверне – на 31-й нед. Частота преждевременных родов до 32 нед. беременности составляет около 1% при одноплодной беременности, 5% – при дихориальной двойне и 10% – при монохориальной двойне. Интересные данные в отношении преждевременных родов были получены нами у пациенток с монохориальной двойней, не осложненной синдромом фето-фетальной гемотрансфузии. Первое – это то, что практически в половине наблюдений отмечалась задержка роста одного или обоих плодов. Второе, как показали наши исследования, частота преждевременных родов была выше у пациенток, родивших нормотрофных детей. По-видимому, уменьшение суммарной массы плодов за счет формирования задержки плода/плодов предотвращает перерастяжение матки и давление на шейку матки и, тем самым, способствует пролонгированию беременности. Это находится в полном соответствии с т.н. теорией «конфликта интересов» при многоплодии: чем больше суммарная масса плодов, тем меньше шансов достичь доношенности и наоборот [8].
Учитывая доказанный на сегодняшний день факт, что длина шейки матки, по данным ТВЭ («золотой стандарт» определения состояния шейки матки), является очень значимым прогностическим критерием для определения угрозы прерывания беременности как при одноплодной, так и многоплодной, во время ультразвукового скрининга у беременных с многоплодием особое значение придается оценке состояния шейки матки для своевременного формирования группы высокого риска в отношении преждевременных родов. Наши исследования, проведенные у 250 беременных с дихориальной и 86 пациенток с монохориальной двойней, показали, что для многоплодной, также как и для одноплодной беременности, у пациенток, родивших в срок, характерно прогрессивное уменьшение длины шейки матки по мере увеличения срока гестации [4]. Меньшая длина шейки матки к сроку родов у пациенток с двойней была обусловлена более высокой понедельной скоростью ее укорочения после 20 нед. беременности: темпы укорочения шейки матки составляли 1,12+0,08 мм/нед. при многоплодной против 0,58+0,06 мм/нед. при одноплодной беременности. У пациенток с двойней, родивших преждевременно, выявлены достоверно более низкие показатели длины шейки матки, начиная с 19-21 нед. беременности, при одноплодной беременности в аналогичной группе пациенток выраженное укорочение шейки матки отмечалось уже в 16-18 нед. (см. рис. 3). Чем короче шейка матки, по данным ТВЭ, тем выше риск преждевременных родов (см. рис. 4). Как и у пациенток с двойней, родивших в срок, мы не выявили достоверных различий в длине шейки матки у пациенток с моно- и дихориальной двойней при преждевременных родах. Исключение составили пациентки с монохориальной двойней, у которых резкое укорочение шейки матки было обусловлено наличием выраженного многоводия у плода-реципиента при синдроме фето-фетальной гемотрансфузии тяжелой степени. Таким образом, определение состояния шейки матки при ТВЭ должно являться обязательным при ультразвуковом скрининговом обследовании пациенток с многоплодием, начиная с 19-20 нед. беременности. Особое внимание следует уделять динамике изменений длины шейки матки с 2-3-недельным интервалом.
 | Рисунок 3: Определение хориальности: а) λ-признак – ДХ; б) Т-признак – МХ. |
 | Рисунок 4: Определение хориальности: а) λ-признак – ДХ; б) Т-признак – МХ. |
Именно длина шейки матки, определенная при ТВЭ, является критерием отбора пациенток для проведения профилактических мероприятий по предотвращению наступления преждевременных родов (токолитики, микронизированный прогестерон, акушерские пессарии).
Вагинальное применение прогестерона было предложено для профилактики преждевременных родов у женщин с укорочением шейки матки, по данным ТВЭ во 2-м триместре беременности на основании его биологических эффектов на шейку матки, миометрий, плодные оболочки [11]. Метаанализ данных по отдельным пациенткам показал, что применение вагинального прогестерона при двойне и длине шейки ≤25 мм приводило к уменьшению, хотя и статистически недостоверному, частоты ПР в сроки до 33 нед. беременности (30,4% против 44,8%; ОР 0,70, 95% ДИ 0,34-1,44). Тем не менее, при применении натурального прогестерона регистрировалось достоверное снижение суммарного показателя неонатальной заболеваемости и смертности (ОР 0,52, 95% ДИ 0,29-0,93). Снижение частоты преждевременных родов на 44% продемонстрировано и в другом многоцентровом исследовании у пациенток с длиной шейки матки, равной 15 мм и менее, при применении вагинального прогестерона (Утрожестан в дозе 200 мг на ночь ежедневно) [7]. В это исследование входили и беременные с двойней, хотя и в меньшем количестве, чем пациентки с одноплодной беременностью. Именно учитывая недостаточное на сегодняшний день количество проанализированных пациенток с многоплодием при применении вагинального прогестерона, многие ученые сходятся во мнении, что существует острая необходимость проведения исследований по определению эффективности прогестерона сугубо для дихориальных двоен.
Что касается акушерских пессариев (АП), а именно широко используемых пессариев доктора Б. Арабин, то недавно в Нидерландах завершилось исследование, в котором 403 женщины с многоплодной беременностью с установленными пессариями сравнивались с 410 пациентками с многоплодием, в отношении которых была избрана выжидательная тактика [6]. Проведенный анализ показал, что среди пациенток с длиной шейки матки ниже 25-й процентили (38 мм) в сроки беременности до 20 нед. профилактическое применение АП сопровождалось достоверным уменьшением количества родов до 32 нед. (14% против 29%; ОР 0,49, 95% ДИ 0,29-0,97) и неонатальной смертности до выписки (2% против 15%; ОР 0,13, 95% ДИ 0,03-0,60). Подбор АП проводится по их внешнему и внутреннему диаметрам, а также высоте искривления с учетом размеров и состояния шейки матки (см. табл. 1). Появление АП в арсенале акушера-гинеколога позволило вместо наложения швов на шейку матки, особенно после 20 нед. беременности, использовать неинвазивный, абсолютно безопасный, высокоэффективный, и в то же время простой, доступный и комфортабельный для пациентки метод. АП играют важную роль в комплексе мероприятий, которые мы в ЦПСиР ДЗ г. Москвы и наши коллеги во всем мире широко применяем для профилактики преждевременных родов как при одноплодной, так и многоплодной беременности.
Таблица 1. Предлагаемые размеры акушерских пессариев во 2-м триместре беременности при двойне, мм.
| Внутренний диаметр | Наружный диаметр | Высота |
|---|
| 32 | 35 | 65 | 70 | 17 | 21 | 25 | 30 | | Без расширения в/зева | | | | | | | | | | – первородящая | + | | + | | | | + | | | –повторнородящая | + | | | + | | | + | | | V- или U-форма в/зева | | | | | | | | | | – первородящая | | + | + | | | | + | | | – повторнородящая | | + | | + | | | + | |
При многоплодной беременности возможно развитие специфических, не характерных для одноплодной беременности, осложнений, основными из которых являются синдром фето-фетальной гемотрансфузии, синдром обратной артериальной перфузии (синдром акардии), внутриутробная гибель одного из плодов.
Синдром фето-фетальной гемотрансфузии (СФФГ), впервые описанный Schatz в 1982 г., осложняет течение 5-10% монохориальных двоен. Несмотря на то, что СФФГ, как правило, наблюдается у пациенток с монохориальной плацентой, необходимо помнить о важных исключениях: сосудистые плацентарные анастомозы описаны и у пациенток с дихориальной монозиготной двойней! Перинатальная смертность при СФФГ в отсутствие внутриутробной коррекции этого осложнения достигает 80-100%. Предполагается, что заболевание развивается вследствие дисбаланса кровотока между двумя монохориальными близнецами из-за наличия плацентарных сосудистых анастомозов. Повышение периферической резистентности плацентарного кровотока способствует шунтированию крови к другому плоду – реципиенту. Таким образом, состояние плода-донора нарушается в результате гиповолемии, которая возникает вследствие потери крови и гипоксии на фоне плацентарной недостаточности, у него развивается анурия и, как правило, задержка роста. К плоду-реципиенту поступает избыточное количество крови из анастомозов в плаценте и у него наблюдается полицитемия. Плод-реципиент компенсирует увеличение объема циркулирующей крови полиурией, состояние его нарушается вследствие сердечной недостаточности, которая развивается в связи с увеличением пред- и постнагрузки на серд-це. Помимо определения стадий СФФГ по R. Quintero, при ультразвуковом исследовании особое внимание должно уделяться эхокардиографии плодов, оценке состояния кровотока в средней мозговой артерии с определением максимальной скорости кровотока. Последнее позволяет оценить выраженность анемии у плода-донора.
В настоящее время единственный радикальный патогенетически обоснованный метод лечения СФФГ – это эндоскопическая лазерная коагуляция сосудистых анастомозов, которая подразумевает максимально возможную «дихорионизацию» плацент [10]. Оперативное вмешательство с использованием техники селективной лазерной коагуляции коммуникантных сосудов при СФФГ с 2005 г. широко проводится в Центре Планирования семьи и Репродукции ДЗ г. Москвы [1]. Эффективность эндоскопической лазеркоагуляционной коррекции СФФГ (рождение хотя бы одного живого ребенка) составляет 65,8%. Но, несмотря на успешно лечение этого специфического осложнения, нередко возникает другая проблема: у 25% пациенток роды произошли в 30-36 нед. Предрасполагающим фактором для преждевременного прерывания беременности, несомненно, является многоводие у плода-реципиента и, как следствие этого, перерастяжение матки. Следует особо подчеркнуть тот факт, что при благоприятном течении двухнедельного интервала после операции беременность удавалось пролонгировать как минимум на 8 нед. Вторым «критическим» периодом в плане преждевременного излития околоплодных вод, развития синдрома анемии-полицитемии и внутриутробной гибели одного из плодов являлись сроки гестации с 28 по 32 нед. Это возможно интерпретировать как следствие прогрессивного нарастания внутриматочного объема за счет увеличения суммарной массы плодов и увеличения по мере прогрессирования беременности диаметра мелких, иногда упускаемых во время операции, анастомозов, что приводит к возникновению рецидива СФФГ или развитию такого послеоперационного осложнения, как синдром анемии-полицитемии плодов.
Более паллиативной тактикой ведения беременных с выраженным СФФГ при отсутствии возможности проведения лазерной коагуляции анастомозирующих сосудов плаценты является амниодренирование избыточного количества околоплодных вод из амниотической полости плода-реципиента. Не устраняя причину СФФГ, этот симптоматический метод лечения, способствует пролонгированию беременности вследствие снижения внутриматочного объема, в определенной мере улучшает состояние как плода-донора, так и плода-реципиента. Однако основным и наиболее важным отличием в перинатальных исходах при проведении лазеркоагуляции анастомозов и амниодренирования является разница частоты неврологических нарушений у выживших детей – 5 против 18-37%.
Синдром обратной артериальной перфузии (синдром акардии) встречается у 1% монохориальных двоен. При синдроме обратной артериальной перфузии плод с акардией/ацефалией (плод-реципиент, паразитирующий) нежизнеспособен, источником его кровоснабжения является кровеносная система второго плода (плод-донор, насос). При этом у плода-донора, как правило, не бывает структурных аномалий. Плод-реципиент – всегда с множественными аномалиями, несовместимыми с жизнью: могут отсутствовать голова и сердце или выявляются значительные дефекты этих органов (рудиментарное сердце). Кровоснабжение плода с синдромом акардии возможно лишь благодаря наличию анастомозов между артериями пуповины плода-донора и плода-реципиента. Характер кровотока к плоду-реципиенту при этом синдроме заключается в том, что оксигенированная кровь поступает к нему не по вене пуповины, как в норме, а через артерию пуповины; деоксигенированная кровь поступает в плаценту по вене пуповины. По мере увеличения срока беременности и с ростом паразитирующего плода у него повышается потребность в оксигенированной крови, что в результате приводит к перегрузке сердца плода-донора с развитием у него явлений сердечной недостаточности. Без проведения внутриутробной коррекции гибель плода-донора наблюдается в 50% наблюдений. Единственная возможность сохранить жизнь плоду-донору – это лигирование пуповины плода-реципиента.
Одним из специфических осложнений при многоплодии является внутриутробная гибель одного из плодов, которая может наблюдаться в любом сроке беременности. Частота поздней (во 2-м и 3-м триместрах беременности) внутриутробной гибели одного из плодов составляет 0,5-6,8% при двойне и 11-17% – при тройне. Основными причинами поздней внутриутробной гибели является при монохориальной плацентации – СФФГ и селективная задержка плода, при дихориальной – задержка роста плода/плодов и оболочечное прикрепление пуповины. Риск последующей гибели второго плода при внутриутробной гибели одного из двойни во 2-м или 3-м триместрах беременности зависит от хориальности: при дихориальном типе плацентации составляет 5-10%, при монохориальности этот показатель достигает 25%. Внутриутробная гибель одного из плодов при дихориальной двойне предполагает возможность выжидательной тактики. Внутриутробная гибель одного из плодов при монохориальной двойне представляет опасность не только для жизни, но и для здоровья живого плода: может развиться синдром эмболизации, что проявляется некрозом тканей или его внутриутробной гибелью. Синдром эмболизации у выжившего плода возникает в результате выраженной гипотонии, связанной с массивным оттоком крови в систему циркуляции погибшего плода через сосудистые анастомозы в единственной плаценте.
Единственный выход для спасения жизнеспособного плода при монохориальной плацентации – это кесарево сечение, произведенное как можно быстрее после гибели одного из плодов. Однако следует учитывать, что экстренное родоразрешение путем операции кесарева сечения не во всех случаях может предупредить развитие неврологических поражений у выжившего плода, особенно если время смерти неизвестно. На более ранних сроках (до достижения жизнеспособности) для спасения оставшегося в живых плода при монохориальной двойне современная тактика подразумевает тщательное динамическое ультразвуковое наблюдение с использованием простого неинвазивного метода – исследование максимальной скорости кровотока в средней мозговой артерии выжившего плода с целью диагностики у него анемии и при необходимости проведения внутрисосудистого переливания крови, что будет способствовать снижению риска формирования гипоксически-ишемического поражения головного мозга.
Данные исследований последних лет доказали необходимость определения максимальной скорости кровотока в средней мозговой артерии при монохориальной двойне для диагностики анемии и при наличии обоих живых плодов [12]. Это обусловлено тем, что даже при отсутствии синдрома фето-фетальной гемотрансфузии возможно развитие синдрома анемии-полицитемии вследствие медленной трансфузии крови через мелкие артериовенозные анастомозы, которые, не приводя к развитию «классического» СФФГ, способствуют медленному оттоку крови от донора к реципиенту.
Таким образом, многоплодие является фактором высокого риска осложнений как для матери, так и для плодов. Учитывая то, что многоплодие рассматривается основным ведущим осложнением ВРТ, в последние годы большое внимание уделяется внедрению так называемой профилактики многоплодия при ЭКО. Внедрение метода SET (single embryo transfer) в ряде стран (Австралия, Великобритания, Канада и др.) привело к значительному снижению ятрогенного многоплодия параллельно увеличению частоты одноплодной беременности, наступившей в результате ЭКО [13]. Однако следует согласиться с мнением ведущих ученых, что достижение оптимальных показателей многоплодной беременности в результате ЭКО невозможно в короткие сроки и в настоящее время многоплодие еще остается проблемой для перинатологов всего мира. Поэтому тщательный ультразвуковой мониторинг на ранних сроках беременности, позволяющий осуществлять дифференцированный подход в зависимости от типа плацентации и характера осложнений, профилактика анемии, гестоза, плацентарной недостаточности, задержки роста плодов, преждевременных родов, своевременная внутриутробная коррекция специфических осложнений многоплодной беременности – основные моменты тактики ведения пациенток с многоплодием, которые, несомненно, способствуют снижению перинатальной заболеваемости и смертности у этой группы беременных высокого риска.
Литература:
1. Бугеренко А.Е., Курцер М.А., Сичинава Л.Г. и др. Акушерство и гинекология. 2013; 10: 40-45.
2. Калашников С.А., Зябликова Р.В., Сичинава Л.Г. Оценка физического развития новорожденных из двойни. Вопросы гинекологии, акушерства и перинатологии. 2004; 3 (3): 55-58.
3. Макацария А.Д., Бицадзе В.О. Профилактика повторных осложнений беременности у пациенток с тромбофилией. М. 2007; 250 с.
4. Сичинава Л.Г., Герасимова А.А., Калашников С.А. и др. Значение ультразвукового мониторинга шейки матки в прогнозировании преждевременных родов при многоплодной беременности. Вопросы гинекологии, акушерства и перинатологии. 2005; 4 (1): 11-14.
5. Сичинава Л.Г., Панина О.Б., Калашников С.А. и др. Многоплодие: диагностика и тактика ведения беременности и родов. Вопросы гинекологии, акушерства и перинатологии. 2002; 1 (2): 47-51.
6. Arabin B., Alfirevic Z. Cervical pessaries for prevention of spontaneous preterm birth: past, present and future. Ultrasound Obstet Gynecol. 2013; 42 (4): 390-399.
7. Fonseca E.B., Celik E., Parra M. et al. Progesterone and the risk of preterm birth among women with a short cervix. N. Engl. J. Med. 2007; 357: 462-469.
8. Multiple Pregnancy. Epidemiology, Gestation and Perinatal Outcome. Editied by I. Blickstein and L.G. Keith. 2005; 976 p.
9. Newman R.B., Luke B. Multifetal Pregnancy. 2000; 275 p.
10. Quintero R.A., Kontopoulos E.V. Ultrasound assessment and Surgical Treatment of Twin-Twin Transfusion Syndrome. J. Matern. Fetal Neonatal Med. 2013; 4 (7): 415-25.
11. Romero R., Nicolaides K., Conde-Agudelo A. et al. Снижение частоты преждевременных родов во 2 триместре беременности и неонатальной заболеваемости в результате вагинального применения прогестерона у женщин с бессимптомным укорочением шейки матки по данным ультразвукового исследования: систематический обзор и метаанализ данных по отдельным пациенткам. Акушерство и гинекология. Новости, мнения, обучение. 2013; 1: 16-37 (перевод).
12. Slaghekke F., Kist W.J., Oepkes D., Pasman S.A., Middeldorp J.M., Klumper F.J., Walther F.J., Vandenbussche F.P., Lopriore E. Twin anemia-polycythemia sequence: diagnostic criteria, classification, perinatal management and outcome. Fetal. Diagn. Ther. 2010; 27 (4): 181-90.
13. Umstad M.P., Hale L., Wang Y.A. et al. Multiple deliveries: The reduced impact of in vitro fertilization in Australia. Austr .and New Zealand J. of Obstetrics and Gynaecology. 2013; 53: 158-164.
References:
1. Bugerenko A.E., Kurtser M.A., Sichinava L.G. i dr. Akusherstvo i ginekologiya. 2013; 10: 40-45.
2. Kalashnikov S.A., Zyablikova R.V., Sichinava L.G. Voprosy ginekologii, akusherstva i perinatologii. 2004; 3 (3): 55-58.
3. Makatsariya A.D. Prevention of recurrent complications of pregnancy in patients with thrombophilia [Profilaktika povtornykh oslozhnenii beremennosti u patsientok s trombofiliei]. Moscow. 2007; 250 s.
4. Sichinava L.G., Gerasimova A.A., Kalashnikov S.A. i dr. Voprosy ginekologii, akusherstva i perinatologii. 2005; 4 (1): 11-14.
5. Sichinava L.G., Panina O.B., Kalashnikov S.A. i dr. Voprosy ginekologii, akusherstva i perinatologii. 2002; 1 (2): 47-51.
6. Arabin B., Alfirevic Z. Cervical pessaries for prevention of spontaneous preterm birth: past, present and future. Ultrasound Obstet Gynecol. 2013; 42 (4): 390-399.
7. Fonseca E.B., Celik E., Parra M. et al. Progesterone and the risk of preterm birth among women with a short cervix. N. Engl. J. Med. 2007; 357: 462-469.
8. Multiple Pregnancy. Epidemiology, Gestation and Perinatal Outcome. Editied by I. Blickstein and L.G. Keith. 2005; 976 p.
9. Newman R.B., Luke B. Multifetal Pregnancy. 2000; 275 p.
10. Quintero R.A., Kontopoulos E.V. Ultrasound assessment and Surgical Treatment of Twin-Twin Transfusion Syndrome. J. Matern. Fetal Neonatal Med. 2013; 4 (7): 415-25.
11. Romero R., Nicolaides K., Conde-Agudelo A. et al. Akusherstvo i ginekologiya. Novosti, mneniya, obuchenie. 2013; 1: 16-37 (translation).
12. Slaghekke F., Kist W.J., Oepkes D., Pasman S.A., Middeldorp J.M., Klumper F.J., Walther F.J., Vandenbussche F.P., Lopriore E. Twin anemia-polycythemia sequence: diagnostic criteria, classification, perinatal management and outcome. Fetal. Diagn. Ther. 2010; 27 (4): 181-90.
13. Umstad M.P., Hale L., Wang Y.A. et al. Multiple deliveries: The reduced impact of in vitro fertilization in Australia. Austr. and New Zealand J. of Obstetrics and Gynaecology. 2013; 53: 158-164.
Current approaches to management of multiple pregnancies
Sichinava L.G.
The Russian National Research Medical University named after N.I. Pirogov of the Ministry of Health of the Russian Federation, Moscow
Abstract: a clinical lecture presents the current management of multiple pregnancies, modern diagnostics and treatment of complications in this high risk group of patients. A different approaches to management of multiple pregnancies according to chorionicity, early diagnosis of specific complications is necessary for improving neonatal outcomes.
Key words: multiple pregnancy, twins, preterm birth, management of twin pregnancy. |
|